루이스 전자점식
덤프버전 :
분류
1. 개요[편집]
길버트 뉴턴 루이스가 고안한 공유 결합을 알아보기 쉽도록 각 원소의 원자가전자들을 기호 주위에 점으로 찍어 표현하는 방법.
2. 그리는 법[편집]
- 각 원소기호를 그린다.
- 원자가전자를 각 원소기호를 중심으로 상하좌우에 하나씩 찍어준다.[1]
- 원자가전자가 5개 이상이면 쌍으로 찍는다.[2]
- 중심원소를 놓고[3] 옥텟 규칙을 만족하도록 바깥 원소와 중심 원소의 홀전자들을 결합해 그리면 된다.[4]
3. 예[편집]
3.1. 물의 루이스 전자점식[편집]
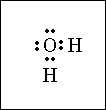
사진에서 전기 음성도가 더 큰 산소가 [math((-))] 전하를 띠게 되는 [math(\rm O-H)] 결합이 비대칭 상태를 이루며 각 결합으로 인한 쌍극자 모멘트가 한 분자 내에서 상쇄되지 않고 남기 때문에 분자 전체적으로 부분적인 전하가 나타나는데 이를 극성이라고 한다. 황화수소([math(\rm H_2S)]), 암모니아([math(\rm NH_3)]) 등도 마찬가지로 쌍극자 모멘트가 분자 내에서 비대칭적으로 분포하기 때문에 극성을 띤다.
3.2. 이산화탄소의 루이스 전자점식[편집]

위의 물과는 달리 비공유 전자쌍이 없는 중심원자 탄소를 기준으로 산소가 직선형(곧은형이라고도 한다)으로 배치되어 있어 쌍극자 모멘트의 합이 0이 되는데 이러한 분자를 무극성이라 한다.[5]
 이 문서의 내용 중 전체 또는 일부는 2023-11-26 02:52:16에 나무위키 루이스 전자점식 문서에서 가져왔습니다.
이 문서의 내용 중 전체 또는 일부는 2023-11-26 02:52:16에 나무위키 루이스 전자점식 문서에서 가져왔습니다.